药品研发是一个漫长、复杂且高度规范化的科学探索过程,通常需要耗费十数年时间和数十亿美元。其全流程可概括为五个核心阶段,而现代计算机软硬件技术已深度融入其中,成为加速创新、提升成功率的关键驱动力。
一、药品研发全流程五大阶段
1. 靶点识别与验证
这是药物发现的起点。研究人员通过基因组学、蛋白质组学等技术,识别与疾病相关的生物分子(如蛋白质、基因),即“药物靶点”,并验证其在疾病机制中的关键作用。
2. 先导化合物发现与优化
针对已验证的靶点,利用高通量筛选、计算机辅助药物设计等方法,从数百万化合物中筛选出具有活性的“苗头化合物”,并进一步化学修饰优化,得到在活性、选择性、药代动力学性质等方面更优的“先导化合物”。
3. 临床前研究
对先导化合物进行全面的实验室与动物研究,评估其药效、毒理、药代动力学及制剂工艺。目的是初步验证其安全性和有效性,为进入人体试验提供数据支持。此阶段会筛选出最具潜力的一个或数个候选药物。
4. 临床研究(I-III期)
在严格监管下进行人体试验,分三期:
- I期:在少量健康志愿者中,主要评估安全性及人体药代动力学。
- II期:在小规模患者群体中,初步探索有效性并进一步评估安全性,确定给药剂量。
- III期:在大规模患者群体中进行随机对照试验,确证疗效与安全性,为药品注册审批提供决定性证据。
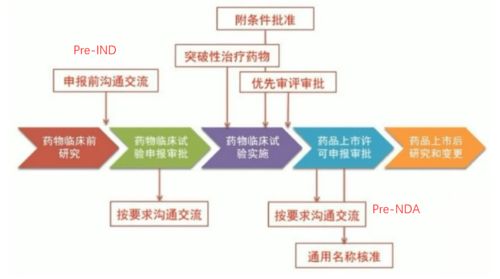
5. 监管审批与上市后监测(IV期)
向国家药品监管机构(如美国FDA、中国NMPA)提交所有研究数据申请上市许可。获批上市后,仍将持续进行IV期临床研究(药物警戒),监测药物在更广泛人群中的长期效果和罕见不良反应。
二、计算机软硬件技术开发的深度融合与支撑
现代药品研发已高度依赖先进的计算技术,主要体现在以下方面:
- 硬件基础:高性能计算(HPC)与云平台
- 高性能计算集群:为分子动力学模拟、量子化学计算、虚拟高通量筛选提供海量算力,使在原子层面研究药物与靶点的相互作用成为可能。
- 云计算平台:提供弹性、可扩展的计算与数据存储资源,使研发团队(尤其是中小型生物技术公司)能够低成本地访问强大的计算能力,并促进跨地域协作。
- 核心软件与算法:从AI到模拟仿真
- 计算机辅助药物设计(CADD):利用分子对接、定量构效关系等方法,在计算机上设计、优化分子结构,大幅缩短先导化合物发现周期。
- 人工智能与机器学习:应用于靶点发现、化合物合成路线预测、患者分层、临床试验结果预测等。深度学习模型能够从海量文献和实验数据中挖掘隐藏规律。
- 生物信息学工具:分析基因组、蛋白质组等组学大数据,识别新的疾病标志物和潜在靶点。
- 临床试验模拟与管理系统:利用仿真技术优化试验设计;CTMS软件则全程管理试验的开展、数据和合规性。
- 数据集成与实验室自动化
- 实验室信息管理系统(LIMS)与电子实验记录本(ELN):实现实验数据的数字化、结构化采集与管理,确保数据完整性、可追溯性,是研发数字化的基石。
- 自动化机器人实验平台:结合调度控制软件,实现7x24小时的高通量实验操作,极大提升实验效率和重现性。
三、趋势与展望:数字化与智能化研发
药品研发正朝着 “数字孪生” 的方向发展,即在虚拟空间中构建从分子到患者群体的全流程数字化模型,用于模拟、预测和优化真实世界的研发活动。人工智能将更深入地贯穿从靶点到上市的全链条,甚至可能颠覆传统的研发范式。软硬件技术的持续创新,特别是量子计算等前沿技术的潜在应用,有望进一步破解生命科学的复杂性难题,最终以更快的速度、更低的成本为患者带来更多突破性疗法。
药品研发的全流程是一条环环相扣、风险极高的科学路径,而现代计算机软硬件技术已从辅助工具演变为核心基础设施。两者的深度融合,正以前所未有的力量推动着医药产业的创新革命。